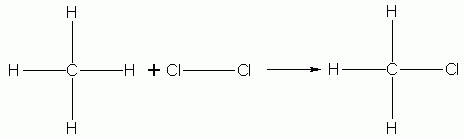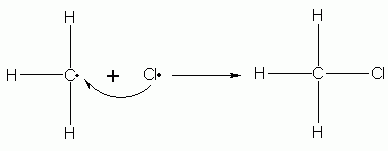Il processo di formazione del cloruro di metano parte dal metano e dal cloro molecolare.
Il cloro, in presenza di luce ultravioletta o di calore, subisce una scissione omolitica e pertanto si dissocia in due atomi radicalici aventi un elettrone spaiato.
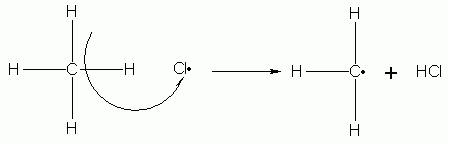
Il radicale cloruro attacca un idrogeno del metano, strappando via l’atomo con l’elettrone. Adesso è il carbonio ibridizzato sp3 ad essere radicalico e, in aggiunta, si forma acido cloridrico.