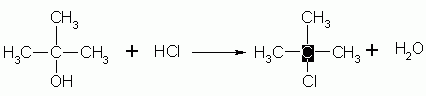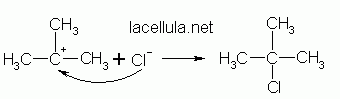alcoli operano reazioni di sostituzione nucleofila Sn1 ed Sn2. Il tipo di reazione tiene conto dell’alcol: se è primario la reazione avrà una cinetica di tipo Sn2, se è terziario la reazione seguirà una cinetica Sn2. Alcoli secondari possono presentare ambedue tipi di reazione.
Le reazioni di sostituzione nucleofila degli alcoli.
| Tipo di alcol | Reazione | Spiegazione |
| Alcol primario | Sn2 | Il carbocatione primario non si forma per motivi di stabilità. |
| Alcol secondario | Sn2-Sn1 | Variabile. |
| Alcol terziario | Sn1 | Più stabili per la formazione del carbocatione |
Reazione di un alcol primario con acido bromidrico: una reazione Sn2.
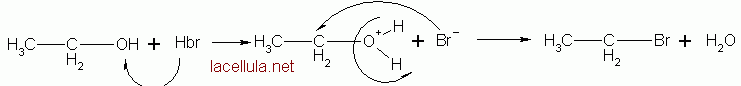
Ponendo a reagire un equivalente di etanolo ed un equivalente di acido bromidrico in soluzione acquosa si forma il bromuro di etile secondo la reazione che segue
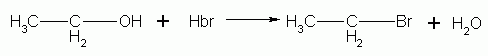
Nella reazione di sintesi l’acido bromidrico protona l’ossidrile dell’etanolo. L’ossigeno cede un doppietto elettronico per formare un nuovo legame e diventa un catione. A questo punto lo ione Br–, che è un nucleofilo, incontra il carbonio, elettrofilo, e forma un legame nello stesso momento in cui l’acqua viene allontanata. In questo modo si forma bromuro di etile ed acqua.
Reazione di un alcol terziario con acido cloridrico: una reazione sn1.
Mettendo a reagire un alcol terziario, come ad esempio il 2-metilpropanolo, con acido cloridrico si ottiene il 2-cloro-2-metilpropano che è un alogenuro alchilico. La sostituzione nucleofila è di primo ordine e si assiste alla formazione di un carbocatione terziario.
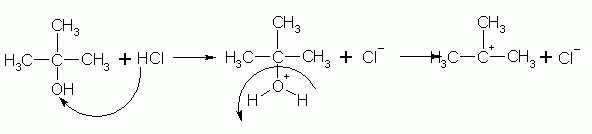
Il primo stadio vede l’attacco di un idrogeno (elettrofilo) all’ossigeno ossidrilico (nucleofilo) per formare un alcol protonato. L’alcol protonato perde una molecola d’acqua e rimane nel sistema il carbocatione terziario con e l’anione cloro.
Nel secondo stadio il cloro (nucleofilo) attacca il carbonio (elettrofilo) per formare la molecola del 2-cloro-2-metilpropano.